Em um laboratório químico, um estudante encontrou quatro frascos (1, 2, 3 e 4) contendo sotuções aquosas incolores de sacarose, KCl, HCl e NaOH, não necessariamente nessa ordem. Para identificar essas soluções, fez alguns experimentos simples, cujos resultados são apresentados na tabela a seguir:
| Frasco | Cor da solução após a adição de fenolftaleína | Condutibilidade elétrica | Reação com Mg(OH)2 |
|---|---|---|---|
| 1 | incolor | conduz | não |
| 2 | rosa | conduz | não |
| 3 | incolor | conduz | não |
| 4 | incolor | não conduz | não |
Dado
Soluções aquosas contendo o indicador fenolftaleína são incolores em pH menor do que 8,5 e têm coloração rosa em pH igual a ou maior do que 8,5.
As soluções aquosas nos frascos 1, 2, 3 e 4 são, respectivamente, de
Clique aqui e faça uma pergunta na sessão de comentários desta questão.
Em cadeias carbônicas, dois átomos de carbono podem formar ligação simples (), dupla (
) ou tripla (
). Considere que, para uma ligação simples, a distância média de ligação entre os dois átomos de carbono é de 0,154 nm, e a energia média de ligação é de 348 kJ/mol.
Assim sendo, a distância média de ligação (d) e a energia média de ligação (E), associadas à ligação dupla (), devem ser, respectivamente,
Clique aqui e faça uma pergunta na sessão de comentários desta questão.
Uma usina de reciclagem de plástico recebeu um lote de ras pas de 2 tipos de plásticos, um deles com densidade 1,10 kg/L e outro com densidade 1,14 kg/L. Para efetuar a sparação dos dois tipos de plásticos, foi necessário preparar 1000 L de uma solução de densidade apropriada, misturando-se volumes adequados de água (densidade = 1,00 kg/L) e de uma solução aquosa de NaCl, disponível no almoxarifado da usina, de densidade 1,25 kg/L. Esses volumes, em litros, podem ser, respectivamente,
Clique aqui e faça uma pergunta na sessão de comentários desta questão.
O monóxido de nitrogênio (NO) pode ser produzido diretamente a partir de dois gases que são os principais constituintes do ar atmosférico, por meio da reação representada por
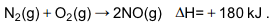
O NO pode ser oxidado, formando o dióxido de nitrogênio (NO2), um poluente atmosférico produzido nos motores a explosão:
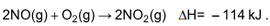
Tal poluente pode ser decomposto nos gases N2 e O2:
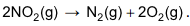
Essa última transformação
Clique aqui e faça uma pergunta na sessão de comentários desta questão.
Volumes iguais de uma solução de I2 (em solvente orgânico apropriado) foram colocados em cinco diferentes frascos. Em seguida, a cada um dos frascos foi adicionada uma massa diferente de estanho (Sn), variando entre 0,2 e 1,0 g. Em cada frasco, formou-se uma certa quantidade de SnI4, que foi, então, purificado e pesado. No gráfico abaixo, são apresentados os resultados desse experimento.
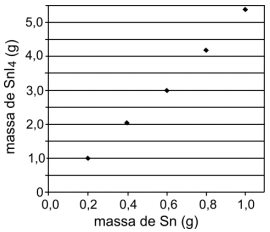
Com base nesses resultados experimentais, é possível afirmar que o valor da relação

é, aproximadamente,
Clique aqui e faça uma pergunta na sessão de comentários desta questão.
A aparelhagem esquematizada na figura abaixo pode ser utilizada para identificar gases ou vapores produzidos em transformações químicas. No frasco 1, cristais azuis de CoCl2 anidro adquirem coloração rosa em contato com vapor d’água. No frasco 2, a solução aquosa saturada de Ca(OH)2 turva-se em contato com CO2 (g).
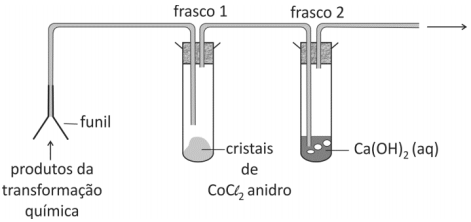
Utilizando essa aparelhagem em três experimentos distintos, um estudante de Química investigou os produtos obtidos em três diferentes processos:
O aparecimento de coloração rosa nos cristais de CoCl2 anidro e a turvação da solução aquosa de Ca(OH)2 foram observados, simultaneamente, em
Clique aqui e faça uma pergunta na sessão de comentários desta questão.
Observe a posição do elemento químico ródio (Rh) na tabela periódica.
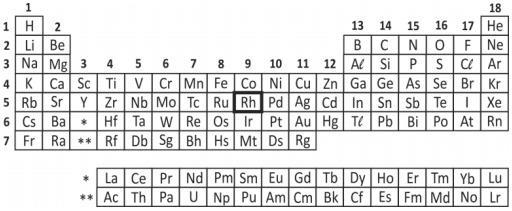
Assinale a alternativa correta a respeito do ródio.
Clique aqui e faça uma pergunta na sessão de comentários desta questão.
Observa-se que uma solução aquosa saturada de HCl libera uma substância gasosa. Uma estudante de química procurou representar, por meio de uma figura, os tipos de partículas que predominam nas fases aquosa e gasosa desse sistema – sem representar as partículas de água. A figura com a representação mais adequada seria
Clique aqui e faça uma pergunta na sessão de comentários desta questão.
A isomerização catalítica de parafinas de cadeia não ramificada, produzindo seus isômeros ramificados, é um processo importante na indústria petroquímica.
A uma determinada temperatura e pressão, na presença de um catalisador, o equilíbrio
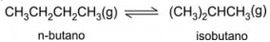
é atingido após certo tempo, sendo a constante de equilíbrio igual a 2,5. Nesse processo, partindo exclusivamente de 70,0 g de n-butano, ao se atingir a situação de equilíbrio, x gramas de n-butano terão sido convertidos em isobutano. O valor de x é
Clique aqui e faça uma pergunta na sessão de comentários desta questão.
A tabela a seguir contém dados sobre alguns ácidos carboxílicos.
| Nome | Fórmula | Ponto de ebulição a 1 atm (ºC) | Densidade a 20 ºC (g/mL) |
|---|---|---|---|
| Ácido etanoico | H3CCO2H | 118 | 1,04 |
| Ácido n-butanoico | H3C(CH2)2CO2H | 164 | 0,96 |
| Ácido n-pentanoico | H3C(CH2)3CO2 | 186 | 0,94 |
| Ácido n-hexanoico | H3C(CH2)4CO2 | 205 | 0,93 |
Assinale a alternativa que apresenta uma afirmação coerente com as informações fornecidas na tabela.
Clique aqui e faça uma pergunta na sessão de comentários desta questão.
Página 3 de 4